Cảnh báo khẩn về thuốc tiêm dự phòng HIV giả mạo trên thị trường
Cục Quản lý Dược thuộc Bộ Y tế vừa đưa ra cảnh báo quan trọng về một loại thuốc tiêm dự phòng HIV có dấu hiệu giả mạo và chưa được cấp phép lưu hành tại Việt Nam. Thông tin này được đưa ra sau khi cơ quan tiếp nhận báo cáo từ Công ty TNHH SNB-REACT Việt Nam về hành vi buôn bán, cung cấp sản phẩm thuốc tiêm mang nhãn hiệu của Công ty Gilead Sciences Inc. nhưng không có giấy phép hợp lệ.
Sản phẩm thuốc giả và nghi vấn về người bán
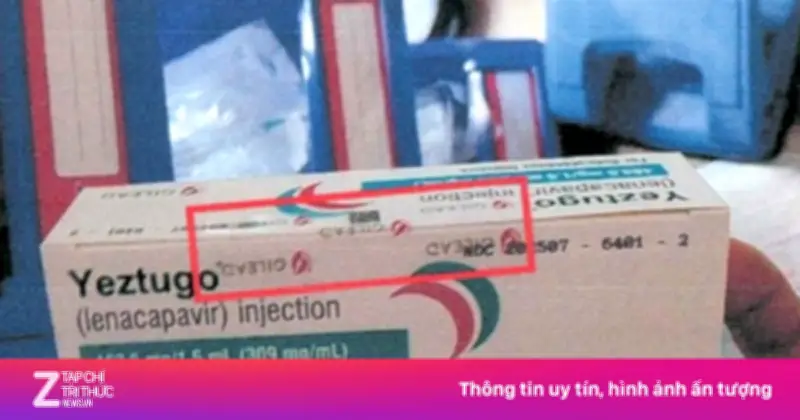
Sản phẩm bị cảnh báo có tên thuốc tiêm YEZTUGO (lenacapavir) injection 463,5 µg/1,5 mL (309 mg/mL), hoàn toàn không có số đăng ký lưu hành. Trên nhãn thuốc ghi sản xuất tại Công ty Gilead Sciences Inc. (Mỹ), nhưng tra cứu trên hệ thống dịch vụ công của Cục Quản lý Dược cho thấy không có sản phẩm nào mang tên này được cấp phép tại Việt Nam.
Theo phản ánh từ Công ty Gilead, người bị nghi ngờ liên quan là ông Trần Thái Học, tự nhận đang làm việc tại Bệnh viện Nhi đồng 1 (TP.HCM) và có liên hệ với Công ty TNHH TH Healthcare. Ông Học đã sử dụng các tài khoản mạng xã hội để quảng bá sản phẩm, đồng thời trực tiếp bán và tiêm thuốc cho người mua với giá 2,5 triệu đồng/mũi/6 tháng.
Đáng chú ý, bao bì sản phẩm do công ty cung cấp cho thấy chưa có thông tin về giấy phép lưu hành và ghi rõ “sản phẩm chưa đăng ký lưu hành, chỉ lưu hành nội bộ”. Tuy nhiên, điều này không hợp lệ vì thuốc chưa được cấp phép tại Việt Nam.
Phản ứng của cơ quan chức năng và bệnh viện
Trước nguy cơ ảnh hưởng đến hiệu quả điều trị và an toàn sức khỏe người dân, Cục Quản lý Dược đã yêu cầu Sở Y tế TP.HCM khẩn trương xác minh, làm rõ và xử lý thông tin liên quan đến sản phẩm giả mạo này. Đồng thời, Sở Y tế các tỉnh, thành phố được đề nghị thông báo tới các cơ sở kinh doanh, sử dụng thuốc và người dân không mua bán, sử dụng sản phẩm trên.
Các đơn vị cần tăng cường kiểm tra, giám sát, kịp thời phát hiện và xử lý các hành vi sản xuất, kinh doanh thuốc giả, thuốc không rõ nguồn gốc. Cục cũng nhấn mạnh việc phối hợp với các cơ quan chức năng để kiểm tra nguồn gốc, hóa đơn chứng từ liên quan, qua đó ngăn chặn kịp thời việc lưu hành thuốc giả trên thị trường.
Đối với Bệnh viện Nhi đồng 1, Cục Quản lý Dược yêu cầu đơn vị kiểm tra, xác minh thông tin liên quan đến nhân sự Trần Thái Học và việc lợi dụng danh nghĩa cán bộ y tế để kinh doanh thuốc trái phép ngoài phạm vi bệnh viện (nếu có).
Trao đổi với báo chí, đại diện Bệnh viện Nhi đồng 1 cho biết ông Trần Thái Học đã nghỉ việc từ ngày 1/5/2025, dù trước đó có công tác tại bệnh viện.
Thu hồi giấy đăng ký 17 loại thuốc tại Việt Nam
Cùng ngày, Cục Quản lý Dược cũng ban hành quyết định thu hồi giấy đăng ký lưu hành 17 loại thuốc tại Việt Nam, theo đề nghị tự nguyện của các cơ sở đăng ký thuốc. Quyết định nêu rõ, các thuốc đã được sản xuất trước ngày quyết định có hiệu lực vẫn được phép lưu hành đến hết hạn dùng. Các cơ sở đăng ký và sản xuất chịu trách nhiệm đảm bảo chất lượng, an toàn và hiệu quả của thuốc trong suốt quá trình lưu hành.
Cục Quản lý Dược yêu cầu Giám đốc Sở Y tế các tỉnh, thành phố, cùng các cơ sở kinh doanh, sản xuất thuốc nêu trên, nghiêm túc thi hành quyết định. Các thuốc thu hồi được đăng ký bởi nhiều công ty, bao gồm:
- Công ty TNHH DRP Inter (TP.HCM): Vidagliptin 50 mg + Metformin 850 mg
- Công ty TNHH Dược phẩm Anh Thy (Hà Nội): Sydakmin Vildagliptin 50 mg, Fynzaf Linagliptin 5 mg, Atbyky Fenticonazol nitrate 200 mg, Qvzan 500 Mesalamin 500 mg, Zalykof Benfotiamin 300 mg, Heboty 2% kem bôi, Zaflyko Ambroxol 30 mg + Clenbuterol 0,02 mg
- Công ty TNHH Thương mại Dược Phú Lâm Trang (Hà Nội): Meqtaz 0,5 mg/ml, Kzygnaf Piracetam 2,4 g
- Công ty CP Dược phẩm Wealphar (Phú Thọ): Carvedilol DWP 3,125 mg, Carvedilol DWP 20 mg, Irbesartan DWP 225 mg, Irbesartan OD DWP 200 mg, Adenosin EC DWP 20 mg
- Công ty CP Dược phẩm CPC1 Hà Nội: Etomidat-BFS 2 mg dung dịch tiêm, Etomidat-BFS 2 mg/ml nhũ tương tiêm
Các thuốc này thuộc nhiều dạng bào chế như viên nén bao phim, viên nang, kem bôi âm đạo, dung dịch tiêm, nhũ tương tiêm, siro và viên nén phân tán trong miệng.
Những động thái này của Cục Quản lý Dược nhằm đảm bảo an toàn dược phẩm, bảo vệ sức khỏe người dân trước các nguy cơ từ thuốc giả và thuốc không đạt chuẩn.









